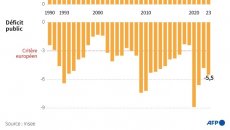
Économie
contenus affichés
-
11:20Sports - Serie A : Une grande première pour un trio arbitral féminin
-
11:13Monde - Mouvement de soutien à Gaza: l'université américaine Columbia ajourne l'évacuation du campus
-
10:59France - Prix de l’électricité : la France 4e grand pays le plus cher, selon une étude
-
10:50Économie - En Chine, Blinken mis en garde contre les pressions américaines
-
08:00Auto - La Grande Collecte du Sport : et si on donnait une seconde vie à notre vélo ?