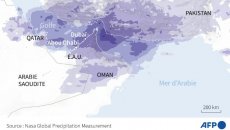
Économie
contenus affichés
-
01:27Monde - Les Etats-Unis bloquent l'adhésion pleine et entière des Palestiniens à l'ONU
-
00:36Monde - Les 12 jurés du procès de Donald Trump à New York ont été sélectionnés
-
00:36Sports - Ligue Europa : La revanche marseillaise, les minots, Di Maria... Les tops/flops d'OM-Benfica
-
00:24Monde - Kenya: le chef des armées et neuf responsables militaires tués dans un crash d'hélicoptère
-
18/04Auto - Stellantis : 36,5 millions d'euros pour Carlos Tavares
Vidéos
Tous publics


Ce corgi a prédit le résultat des quarts de finale de la Ligue des champions
19 avril 2024 - BFMTV